Schwarzwasser
Schwarzwasser
Schwarzwasser und typische Schwarzwasserfische haben bei einigen Aquarianern einen ganz besonderen Ruf. Vor einigen Jahren, als es noch das tolle DATZ-Forum in Stuttgart gab, das herbstliche aquaristische Ereignis in der Bundesrepublik, hielt ich einen Vortrag über Schwarzwasser und dessen Wirkung auf die Physiologie der Fische. Die weichen, teilweise sogar extrem mineralarmen, durch Huminstoffe dunkelbraun gefärbten Gewässer aus Südamerika, Zentralafrika oder Asien kennt wohl jeder, der schon länger die Aquaristik etwas intensiver betreibt. Gerade im Zusammenhang mit den Gewässern des zentralen Amazoniens ist die Unterteilung der drei häufigsten Gewässertypen Weißwasser, Klarwasser und Schwarzwasser in Wissenschaft und Aquaristik gut etabliert (Born 1956, Geisler 1964).

Fische aus dem letzteren dieser Gewässertypen, dem Schwarzwasser, erweisen sich, zumindest bei der Eingewöhnung, oft als empfindlicher als andere amazonische Fische. Eine Erklärung dafür wurde immer damit begründet, dass sich die Fische im Laufe der Evolution an die Wasserwerte angepasst hätten. Ich konnte in meinem Vortrag und in einem dazu erschienen Beitrag in der DATZ – hoffentlich – mit der weit verbreiteten Ansicht aufräumen, dass Schwarzwasserfische das Schwarzwasser zum Leben unbedingt brauchen. Vielmehr ist es, zumindest aus wissenschaftlicher Sicht, so, dass einige – besser angepasste – Arten im Schwarzwasser überleben können.
Aber der Reihe nach …
Was ist Schwarzwasser?
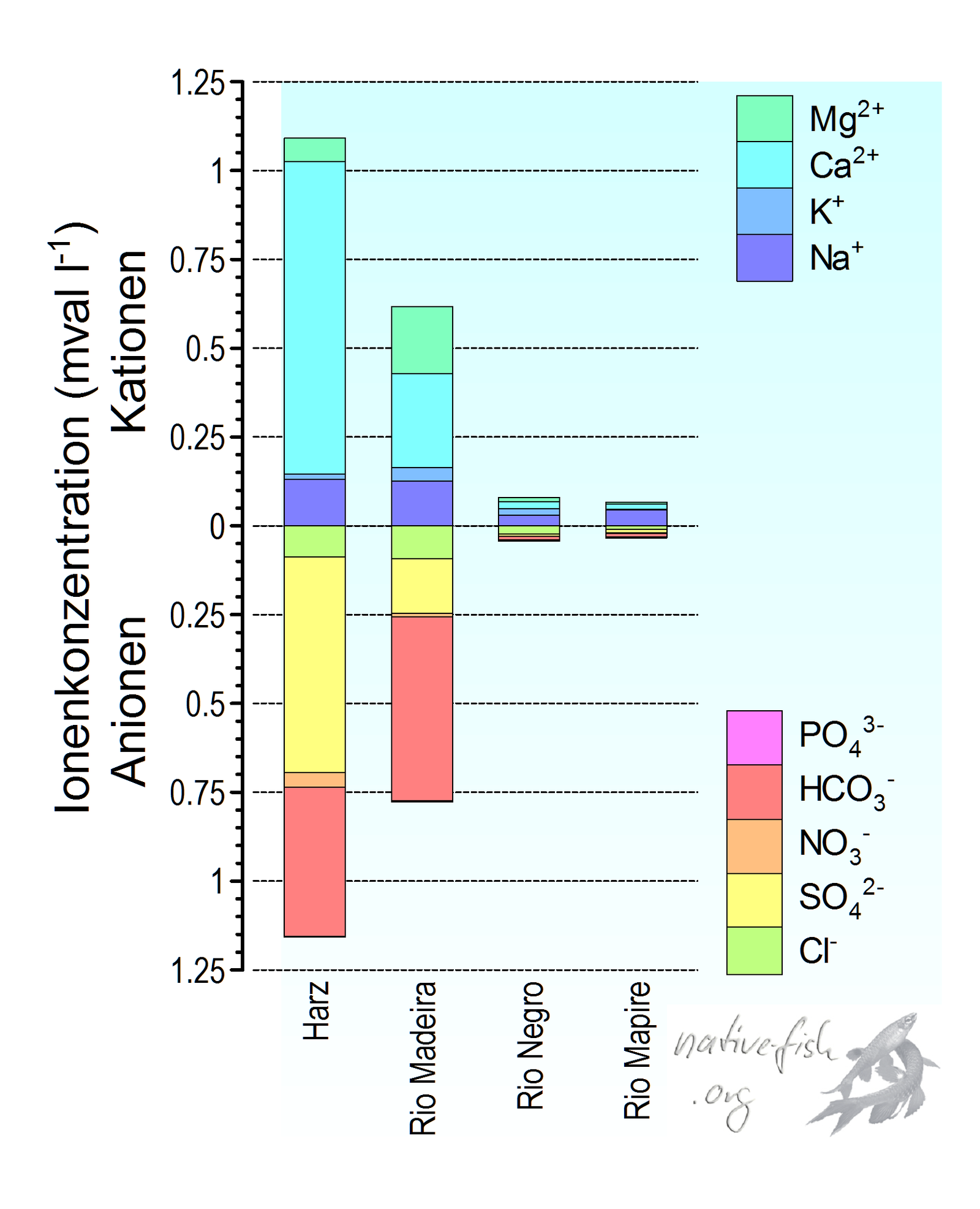
Schwarzwasser zeichnet sich hauptsächlich durch die folgenden Besonderheiten aus: Es ist aufgrund seiner geologischen Herkunft sehr arm an Kationen wie Natrium (Na+), Kalium (K+), Calcium (Ca2+), Magnesium (Mg2+) sowie Anionen wie Chlorid (Cl – ), Sulfat (SO42- ) und Hydrogencarbonat (HCO3- ) und damit natürlich auch sehr weich und leitet den elektrischen nur Strom sehr schlecht (Kuchler et al. 2000).
Die Podsole (Bleicherden) des südamerikanischen Kontinents sind der Schlüssel zu den speziellen Gegebenheiten des Schwarzwassers. Diese Böden entwickeln sich aus der Verwitterung eines sehr silikatreichen Gesteins (Quartz-Podsole). Sie besitzen nur eine sehr geringe Wasserhaltefähigkeit, kaum verwitternde Substanzen, die Ionen abgeben können sowie sehr wenige Tonminerale. Das Wasser dringt deshalb in den Boden ein und nimmt Huminstoffe mit. Es kommt zu einer Versauerung der Böden.

Nicht immer sind alle Flüsse in einem Gebiet reine Schwarz-, Weiss- oder Klarwasserflüsse. So können auch in Weisswassergebieten, die sich vor allem im Bereich der Anden befinden, kleine und mittlere Gewässer völlig unterschiedliche Gewässertypen aufweisen.

Durch das Fehlen von anorganischen Puffersubstanzen und durch seinen hohen Anteil an komplexen organischen Säuren wie Huminstoffen (Geisler 1953, Geisler 1955, Geisler 1972) reagiert das Wasser sehr bis – zumindest im aquaristischen Sinn – extrem sauer. Diese Huminstoffe, in der Summe als DOC (Dissolved Organic Carbon, also gelöster organischer Kohlenstoff) zusammengefasst, absorbieren das Licht vor allem im blauen und ultravioletten Bereich des sichtbaren Lichtspektrums, weshalb dieses Wasser gegen den weißen Sand auch rot bis braun erscheint.
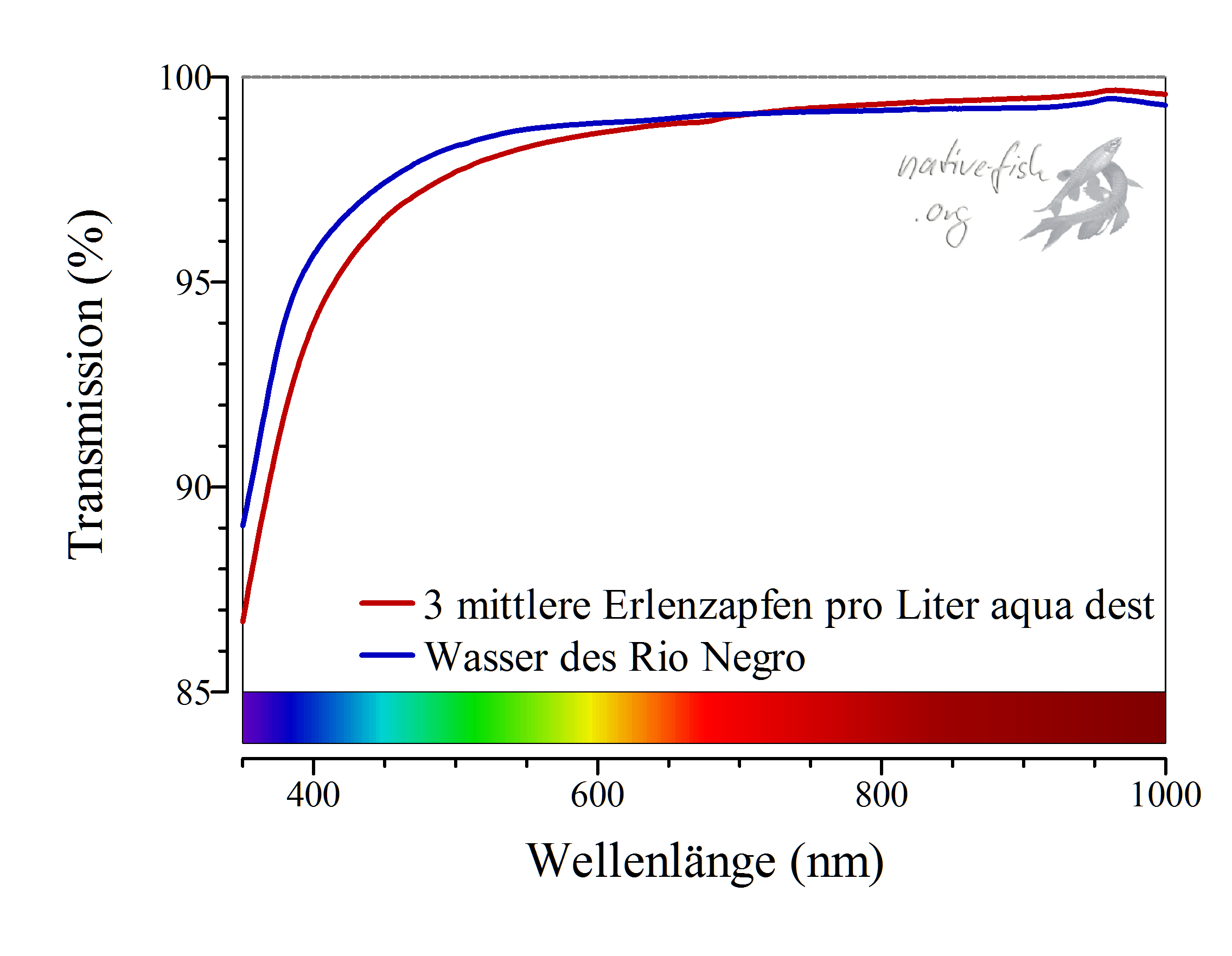
In der obigen Abbildung wird ersichtlich, dass der blaue Bereich des Lichtspektrums weniger stark durchgelassen wird (Transmission ist geringer), während der Rotanteil sehr stark durchgelassen wird. Deshalb wirkt das Wasser auch rot bis braun, wenn man es in einer Tiefe von wenigen zehn Zentimetern gegen einen weißen gut reflektierenden Hintergrund, zum Beispiel weißen Sand, betrachtet.

Bedingt durch das Fehlen des blauen Anteils am photosynthetischen Spektrum wird das Wachstum höherer Pflanzen teilweise gehemmt. Als Folge des hohen Gehalts an Huminstoffen und Gerbsäuren wird auch die immer wieder die extreme Keimarmut des Schwarzwassers hervorgehoben (Geisler 1955, Geisler 1954). Folgende Charakteristika zeichnen Schwarzwasser aus:
Charakteristika des Schwarzwassers:
- Ionenarmut
- niedriger pH
- hohe Huminstoffkonzentration
- Keimarmut
Aus dem Rio Negro Einzug wurde im Jahre 2000 eine Arbeit publiziert, die viele Parameter des Schwarzwassers an verschiedenen Fundorten auflistete (Kuchler et al. 2000). Eine Auswahl der Analysen ist in der folgenden Tabelle wiedergegeben. Die relevanten Extremwerte (Minima und Maxima) sind rot hervorgehoben.
| Probennahmeort | — — | DOC-Konz. | — — | pH | — — | el. Leitfähigkeit | |
|---|---|---|---|---|---|---|---|
| (mg/l) | (µS/cm) | ||||||
| Igarapé Inácio (near Manaus) | 17.5 | 4.05 | 28.6 | ||||
| Rio Negro (near Manaus) | 7.8 | 5.01 | 9.9 | ||||
| Rio Negro (at Manaus) | 7.7 | 5.80 | 8.9 | ||||
| Rio Demini (below Araçá) | 14.1 | 3.96 | 14.7 | ||||
| Rio Marauiá | 6.1 | 5.51 | 9.5 | ||||
| Rio Tea | 14.7 | 3.89 | 24.4 | ||||
| Rio Uneiuxi | 12.7 | 4.08 | 21.9 | ||||
| Rio Daraá | 18.6 | 3.91 | 27.7 | ||||
| Rio Branco | 2.7 | 6.07 | 10.0 |
Diese vier wesentlichen Faktoren Ionenarmut bzw. niedrige elektrische Leitfähigkeit, niedriger pH, hohe Konzentration von Huminstoffen und Keimarmut scheinen also ein Schlüssel zu den Problemen bei der Eingewöhnung und erfolgreichen Haltung von Fischen aus dem Schwarzwasser zu sein. Nachfolgend werden diese Parameter deshalb aus der Sicht der Fische betrachtet.

Wie nehmen Fische Wasserparameter wahr?
Wenn wir uns mit dem Problem der obigen vier Faktoren für die Fische beschäftigen wollen, müssen wir uns mit den Funktionen der Kiemen, dem zentralen Organsystem für den Austausch des Fisches mit seiner Umgebung, auseinandersetzen.
Kiemen dienen nicht nur der Atmung, indem sie sehr effizient Sauerstoff aus dem Umgebungswasser aufnehmen können, sondern sind auch zusätzlich Organe der Ionenregulation, der Säure-Basen-Regulation (einer Sonderform der Ionenregulation) der Exkretion (von Endprodukten des Stickstoffstoffwechsels) und der Osmoregulation (Evans et al. 2005). Die Niere spielt bei Knochenfischen im Süßwasser, anders als etwa bei landlebenden Wirbeltieren, eine eher untergeordnete Rolle (Evans 1981, Kirschner 1981, Willmer et al. 2005, Withers 1992).

In der aquaristischen Literatur wurde mehrfach auf das Problem der Osmoregulation bei Fischen in Süßwasser hingewiesen. Da die Kiemen zum Zweck einer optimalen Sauerstoffaufnahme sehr großflächig und dünn sein müssen und dazu immer von relativ großen Volumina frischen Wassers durchströmt werden, gelangt Wasser vor allem auf diesem Weg osmotisch in den Fisch hinein (1). Die Fische müssen dabei – die im Wasser gelöste Menge an Sauerstoff ist ca. um den Faktor 30 geringer als in Luft – (Dejours 1975) recht große Wassermengen durch die Kiemen bewegen. Diese großen Mengen führen zu einer hohen osmotischen Wasseraufnahme und zu einem deutlichen Ionenverlust. Die Haut der Fische ist für Wasser vergleichsweise undurchlässig und Süßwasserfische trinken nicht aktiv, hier kommt es also nicht zu einer Wasseraufnahme.
Ionen gelangen vor allem über die Nahrung in den Fisch (2). Der Ionenverlust der Fische wird normalerweise über die Nahrung ausgeglichen, was aber während der Trockenzeiten, wenn sehr viele Fische in sehr wenig Wasser mit noch weniger Nahrung schwimmen, sehr schwierig sein kann. Raubfische sind dann überlegen, da sie die von ihnen benötigten Ionen mit den gefressenen Fische aufnehmen können. Eine aktive Aufnahme von Ionen kann aber auch direkt über die Kiemen erfolgen. Dazu weiter unten mehr.
Ein weiterer Ionenverlust tritt auf, wenn das über die Kiemen in den Fisch eingedrungene Wasser als Urin abgegeben wird (3). Der Urin fällt zum Teil in sehr großen Mengen an und erreicht zum Teil zwischen 30 und 70% des Körpergewichts pro Tag (Wilkie 2002). Mit dieser Harnabgabe kommt es zu einem weiteren teilweisen Verlust von Ionen.

Aus den obigen Ausführungen wird also deutlich, dass der Ionenverlust in tropischen Weichwassergebieten ein Problem für Tiere darstellen kann. Viele Tiere nehmen deshalb jede Möglichkeit wahr, Ionen aufzunehmen.
Welche Ionen sind wichtig?
Beim Menschen gibt man bei einem Blutverlust, wenn keine geeigneten Blutkonserven zur Hand sind, zunächst eine 0.9 %ige Kochsalzlösung. Die wichtigsten Ionen im Blutplasma sind bei Fischen wie bei uns Menschen Natrium (Na) und Chlorid (Cl), also Kochsalz. Deren Konzentration beträgt im Blutplasma, dem wässrigen Anteil der Blutes, bei Na+ ungefähr 150 mmol -1 und bei Cl- ca. 110 mmol l-1 (Willmer et al. 2005). Millimol pro Liter (mmol l-1) ist ein in der Wissenschaft verwendeter Begriff für Konzentrationsangaben, welcher die Teilchenzahl berücksichtigt. val bzw. mval sind Angaben, welche die Konzentration und die Ladung berücksichtigen. Diese Ionen liegen im Schwarzwasser, welches in Amazonien sehr weich bzw. ionenarm ist, in ungefähr 5000-fach geringerer Konzentration als im Blutplasma vor, z.B. 19 bzw. 21 µmol l-1 im Leitungswasser des INPA in Manaus (Wood et al. 2003).
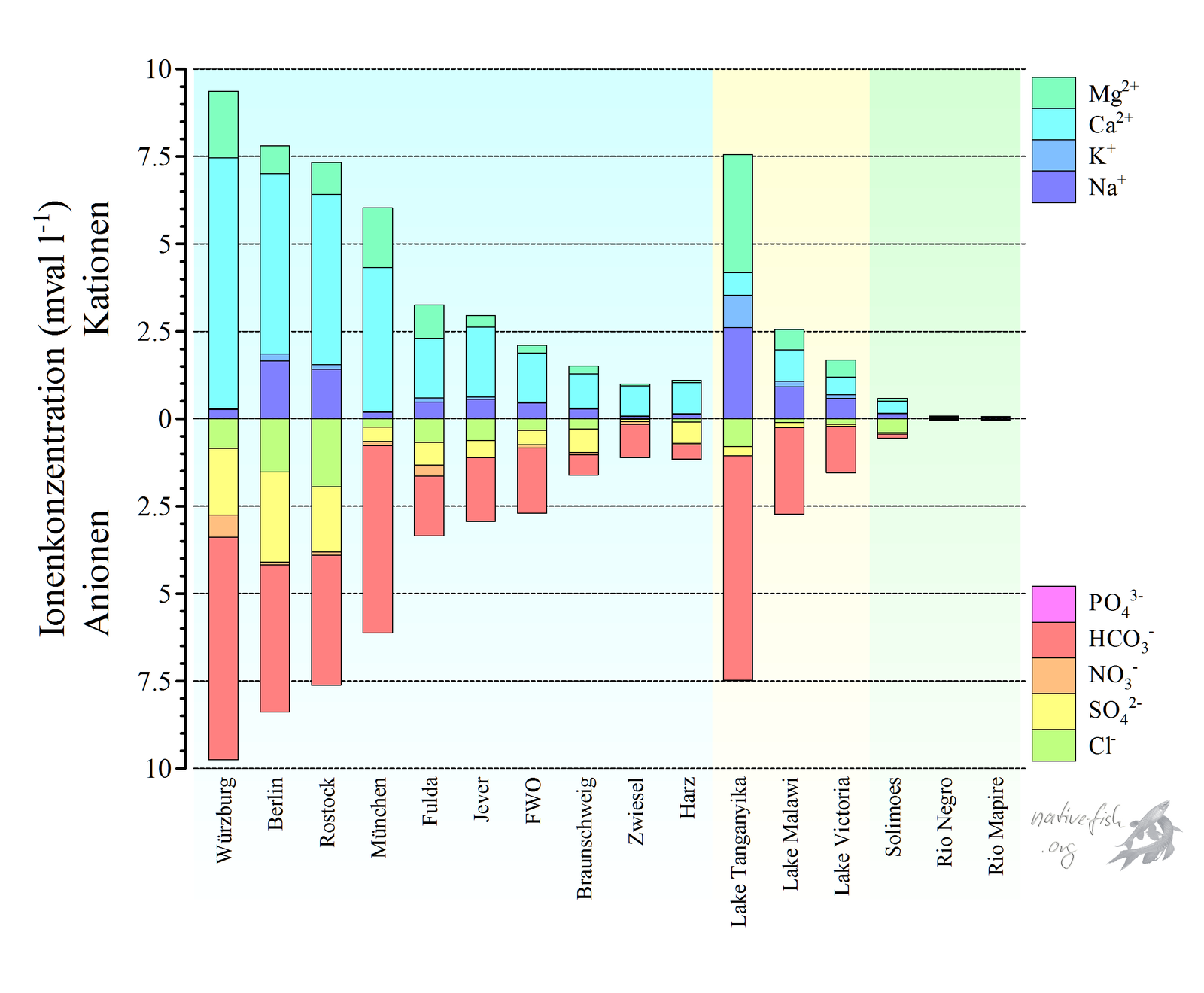
Die Ionenverluste der Fische können natürlich über die Aufnahme von Nahrung und deren anschließende Resorption über den Darm vollständig oder teilweise kompensiert werden. Leider gelingt bei kleinen Tieren, die ein sehr ungünstiges (also großes) Verhältnis von Körperoberfläche zu Körpervolumen aufweisen, die ausschließliche Kompensation über die Nahrung nicht immer, weshalb sich bei verschiedenen wasserlebenden Tieren diverse Transportsysteme in den Zellen herausgebildet haben, die es teilweise erlauben, selbst noch aus extrem stark verdünnten Lösungen (wie z.B. Schwarzwasser) Ionen aktiv unter Energieverbrauch aufzunehmen, so dass die Ionenaufnahme den Ionenverlust übersteigt.
Ionenregulation über die Kiemen – die meisten Fische können das sehr gut
Diese ionenregulatorischen Prozesse finden in den sogenannten „Chloridzellen“ direkt im Kiemenepithel statt (Laurent und Dunel 1980, Perry 1997). Die Aufnahme von Ionen ist ein aktiver, ATP verbrauchender Prozess. In den spezialisierten Chloridzellen, die zwischen 10 und 20 % der Kiemenepithelzellen ausmachen können, transportieren die „Ionenpumpen“ unter erheblichem Energieaufwand bestimmte Ionen (Na+, Ca2+, K+, H+, Cl- , HCO3- , …) gegen einen starken Konzentrationsgradienten über das Kiemenepithel in den Fisch hinein bzw. aus dem Fisch hinaus während sie an anderen Stellen der Kiemen aber – wie oben dargestellt – auch passiv Ionen verlieren können.
Die Ionenregulation über die Kiemen von Fischen weist in seinen Grundsätzen sehr große Ähnlichkeiten mit der Ionenregulation des Menschen in der Niere auf. Einige Fische (darunter Schwarzwasserarten und Killifische) sind deshalb zu Modellorganismen für die Ionenregulation in der biomedizinischen Forschung geworden.
Der Anteil von Chloridzellen und damit die Fähigkeit zur Ionenregulation kann recht schnell (innerhalb weniger Tage) deutlich ansteigen, wenn Fische zum Beispiel in destilliertes Wasser verbracht werden (Fernandes und Perna-Martins 2002, Moron et al. 2003). Neuere Untersuchungen weisen allerdings auch auf die Beteiligung anderer Zelltypen im Kiemenepithel beim Ionenaustausch hin (Perry et al. 2003).
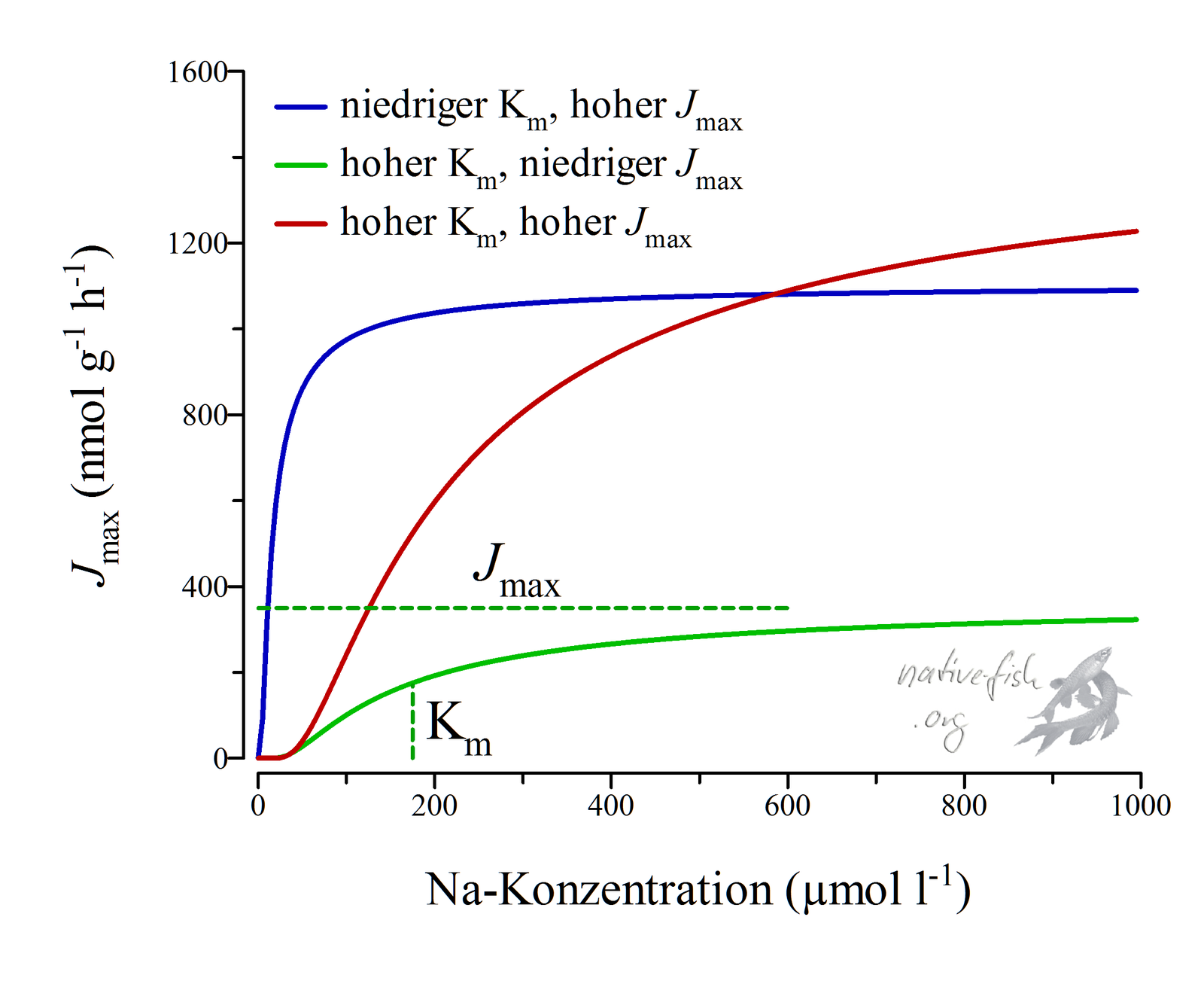
Die Aufnahme und Abgabe von Ionen wird gemessen, indem die zu untersuchenden Fische in Wasser mit einer bestimmten – meist sehr geringen – Ionenkonzentration gesetzt werden. Nach einer gewissen Zeit werden die vom Fisch abgegebenen und die über die Kiemen aufgenommenen Ionen gemessen. Zur Unterscheidung der Aufnahme und Abgabe der Ionen werden oft radioaktiv markierte Ionenspezies verwendet. Sonst könnte man ja auch nicht unterscheiden, welche Ionen aufgenommen und welche Ionen abgegeben wurden.
Für die Abschätzung der Leistungsfähigkeit der Ionenaufnahme kommen zwei Größen zum tragen. Jmax gibt die maximale Aufnahmerate wieder, also die “Geschwindigkeit”, mit der Ionen aufgenommen werden können. Km ist ein Maß für die Affinität der Transporter zu den Ionen. Die Größe gibt an, welche Konzentration der Ionen nötig ist, um diese noch mit der Hälfte der maximalen Geschwindigkeit aus dem Wasser aufnehmen zu können. Je geringer also Km, desto leichter fällt es dem Fisch auch noch aus extrem ionenarmen Gewässern Ionen aufzunehmen. Je höher Jmax ist, desto mehr Ionen können bei freier Ionenverfügbarkeit in einer gewissen Zeit vom Fisch aus dem Wasser aufgenommen werden. Die beiden Parameter sind jedoch nicht notwendigerweise miteinander korreliert.
Die folgenden Daten für die Aufnahme von Natriumionen sind aus der Arbeit von Gonzalez et al. (2002) entnommen. Auch hier sind die Extremwerte farbig markiert.
| Art | — — | Fischgruppe | — — | Km | — — | Jmax | |
|---|---|---|---|---|---|---|---|
| (µmol/l) | (nmol/g h) | ||||||
| Carnegiella strigata | Salmler | 32.5 | 1225.0 | ||||
| Gymnocorymbus ternetzi | Salmler | 27.7 | 691.3 | ||||
| Hemigrammus sp. | Salmler | 30.9 | 1440.0 | ||||
| Paracheirodon axelrodi | Salmler | 53.7 | 773.0 | ||||
| Paracheirodon innesi | Salmler | 12.9 | 448.2 | ||||
| Corydoras julii | Welse | 147.8 | 3604.6 | ||||
| Pimelodus sp. | Welse | 29.7 | 1263.9 | ||||
| Apistogramma A | Buntbarsche | 258.5 | 1752.5 | ||||
| Geophagus sp. | Buntbarsche | 111.8 | 1154.5 | ||||
| Pterophyllum scalare | Buntbarsche | 136.1 | 428.0 | ||||
| Satanoperca jurupari | Buntbarsche | 276.7 | 457.1 |
Die in der Arbeit untersuchten Salmlerarten zeigten also eine deutlich leistungsfähigere Ionenregulation als vergleichbare Buntbarscharten. Der Km für den Neonsalmler liegt um den Faktor 10000 niedriger als die Natriumionenkonzentration im Blutplasma der Art.

Warum sind diese Fische so gute Ionenregulierer? Dazu wären mehrere Erklärungen möglich: Ökologisch sind viel kleine Salmlerarten auch auf pflanzliche Anflugnahrung angewiesen, die nicht immer alle wichtigen Ionen enthält. Vielleicht sind sie deshalb bessere Ionenregulierer. Buntbarsche ernähren sich hingegen oft von tierischer Nahrung. Einige größere Arten sind sogar Räuber, welche die Ionenregulation ihrer Beute überlassen können! Stammesgeschichtlich sind Buntbarsche sekundäre Süßwasserfische, deren Vorfahren aus dem Meer – einem ionenreichen Milieu – kamen, Salmler sind hingegen primäre Süßwasserfische. Und nicht zuletzt sind die in der Tabelle verglichenen Salmler kleiner, als die aufgeführten Cichliden. Die Größe und Form der Fische sowie die damit einhergehende Relation von Oberfläche zu Volumen könnte also auch einen Effekt bedingen.
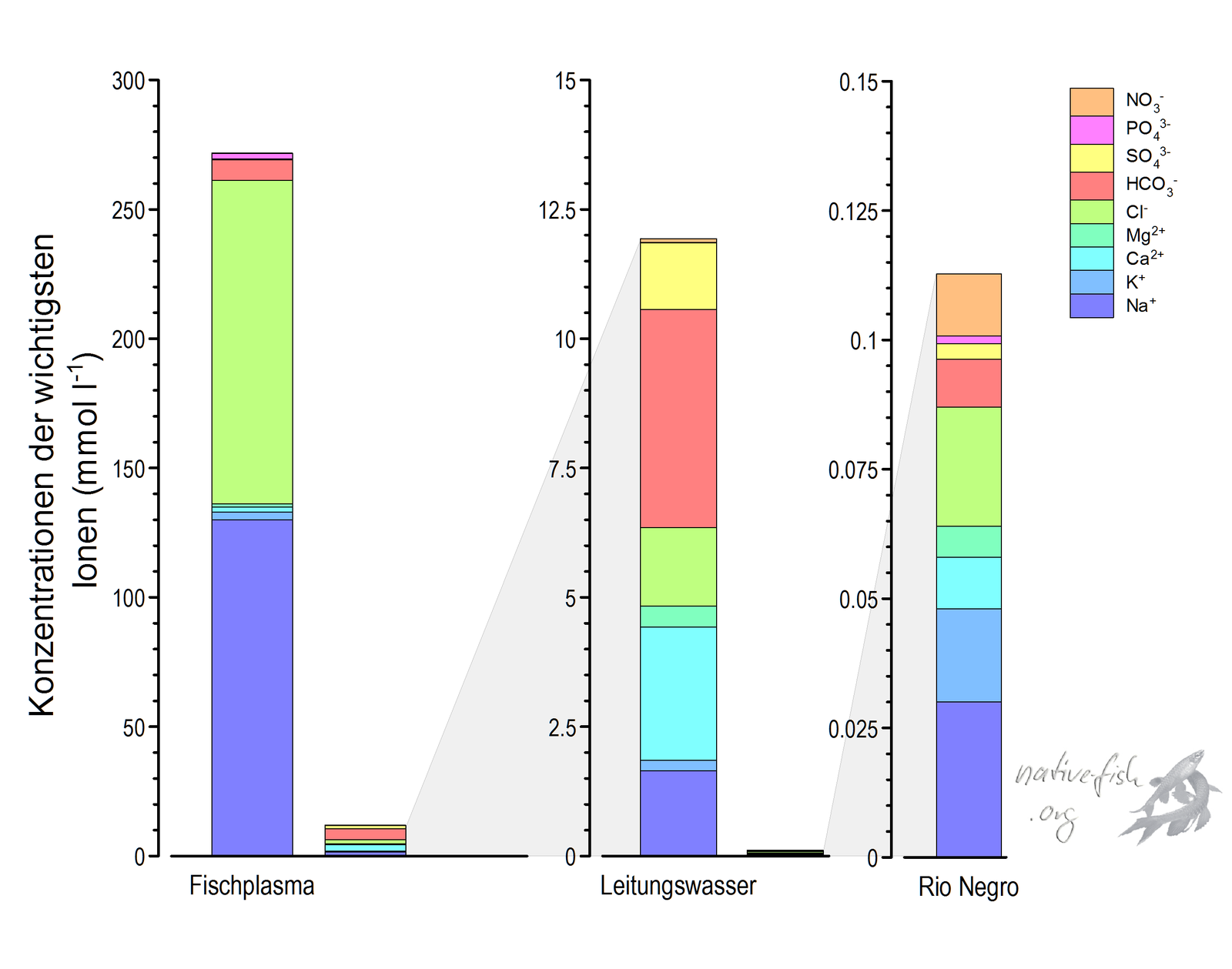
Die Möglichkeit und die Regulation der aktiven Aufnahme von Ionen gegen einen extrem großen Gradienten scheint also Schwarzwasserbewohner auszuzeichnen. Wir müssen dabei aber bedenken, dass diese bessere Regulationsfähigkeit von Schwarzwasserbewohnern aus physiologischer Sicht einen deutlichen Vorteil (keinen Nachteil!) in ionenarmen Gewässertypen darstellt, der hingegen in ionenreicheren Gewässern kein Nachteil ist!
Ein weiterer Faktor, der Schwarzwässer auszeichnet, ist der teilweise extrem niedrige pH. Die Konzentrationsunterschiede von H+-Ionen im Schwarzwasser (pH 4 oder noch darunter) und dem Fischblut (pH 7.8 – 8.1) sind sehr hoch. Ein pH-Unterschied von 4 macht also in den Konzentrationsunterschieden einen Faktor von 10000:1 oder noch größer aus. Diese großen Unterschiede treten vor allem dann auf, wenn die Fische in extrem sauren Habitaten leben (Hirata et al. 2003) und der pH- Unterschied zwischen Plasma und Umgebung also 4 oder sogar noch mehr Einheiten entspricht (Hirata, 2003). Da Lösungen von Ionen versuchen, ihre Konzentrationen passiv durch Diffusion auszugleichen, dachte man bisher, das Problem sei, dass aus den Fischen die Na+-Ionen ausströmen und möglicherweise im Gegenzug H+-Ionen vom Wasser in die Fische einströmen. Ca2+-Ionen, die im Schwarzwasser ebenfalls in nur extrem geringen Konzentrationen vorkommen, besitzen einen regulatorischen Einfluss auf den Ionenverlust über die Kiemen. Extrem geringe Calciumkonzentrationen wie im Schwarzwasser führten im Versuch zu einem Anstieg des Ionenverlustes über die Kiemen. Ich hatte über diese Vorgänge schon an anderer Stelle berichtet (Hetz 2003).
pH-Regulation
Obwohl in der Aquaristik dem pH besondere Beachtung zuteil wird, sind die Protonen (H+) nichts anderes als Ionen in sehr geringer Konzentration. Die pH-Regulation ist also nichts anderes als eine besondere – und komplexe – Form der Ionenregulation. Versuche zeigten zunächst, dass die untersuchten Fische bis zu einem gewissen pH-Bereich in der Lage sind, netto mehr Na+ aufzunehmen als sie verlieren (Gonzalez et al. 2002). Diese Fähigkeit ist besonders bei sauren pH-Werten ausgeprägt und wird offenbar auch durch niedrige pH-Werte (hohe H+-Konzentrationen) stimuliert. So kann z.B. der Trauermantelsalmler Gymnocorymbus ternetzi bei pH 5 seine Natriumaufnahme auf das vierfache im Vergleich zu pH 6.5 steigern (Gonzalez, 1997). Diese Fähigkeit ist wichtig, da der Verlust an Natriumionen über die Kiemen mit sinkendem pH stark ansteigt. Allerdings können Trauermantelsalmler den Ionenverlust bei pH 4 nicht mehr ausgleichen und sterben nach relativ kurzer Zeit, wenn man ihnen nicht gestattet, fehlende Ionen über die Nahrung aufzunehmen. Wildfänge von Neonsalmlern (P. innesi) hingegen überstehen sogar mittelfristig (einige Tage) pH-Werte von 3.5 oder 3.0 im Experiment. Bei Neonsalmlern konnte selbst bei pH 4.0 oder 3.5 kein Nettoverlust an Natriumionen festgestellt werden (Gonzalez und Preest 1999). Irgendwie scheint aber bei einem Konzentrationunterschied von vier Größenordnungen, also dem Faktor 10000 die Grenze zu liegen.

Schwarzwasserfische scheinen also noch deutlich besser an niedrigere pH-Werte angepasst zu sein als „normale“ Weichwasserfische. Bei Neonsalmlern schien das Calcium keine große Rolle bei der Regulation des Natriumverlustes zu spielen, wogegen es bei Skalaren (Pterophyllum scalare) einen großen Effekt zeigt (Gonzalez und Wilson 2001). Es lässt sich also keine allgemeine Aussage treffen. Halten wir aber dennoch fest, dass der niedrige pH von Schwarzwasserfischen besser toleriert wird als von anderen Fischen, also auch diese Fähigkeit einen deutlichen Vorteil von Schwarzwasserfischen ausmacht. Es ist aus physiologischer Sicht jedoch keinesfalls so, das Schwarzwasserfische einem niedrigen pH „brauchen“. Nur am Rande bemerkt: Der pH spielt auch bei der Sauerstoffaufnahme und dem Sauerstofftransport des Hämoglobins in den roten Blutkörperchen eine wichtige Rolle. Bei niedrigem Plasma-pH sinkt die Affinität des Hämoglobins zum Sauerstoff (Nikinmaa 2001, Pelster und Decker 2004) und das Blut kann weniger Sauerstoff transportieren.
Spielen also Huminstoffe als dritte wesentliche Eigenschaft des Schwarzwassers eine größere Rolle als bisher vermutet? Zufällig machten kanadische Wissenschaftler bei Versuchen zur Ionenregulation von Fischen direkt auf dem Rio Negro die Erfahrung, dass sich die Ergebnisse ganz anderes verhalten können, wenn „natürliches“ Schwarzwasser aus dem Rio Negro statt definiertem Weichwasser aus dem Labor verwendet wird (Gonzalez et al. 2002). Deutlich abgeschwächte Ionenverluste in natürlichem Rio Negro- Wasser bei Corydoras, Pimelodus, Hemigrammus, Carnegiella, Geophagus und Apistogramma wiesen auf Schutzwirkungen der chemisch sehr schwer definierbaren Huminsäuren hin. Alle Huminstoffe und andere Kohlenstoffverbindungen werden deshalb unter dem Sammelbegriff „dissolved organic carbon“, kurz: DOC zusammengefasst.
Dissolved Organic Carbon, (DOC), ist ein Summenparameter, der angibt, in welcher Konzentration organische Kohlenstoffe im Wasser vorliegen. Diese organischen Kohlenstoffe liegen zum großen Teil als Huminstoffe vor und sind ein wichtiges Charakteristikum des Schwarzwassers.
Ob sich Huminstoffe direkt auf den Ionenverlust auswirken oder einen mittelbaren Effekt über die Komplexierung des Calciums ausüben, ist nicht bekannt. Halten wir also fest, dass Huminstoffe zwar einen positiven Effekt, auf Ionen- und pH-Regulation ausüben können was wiederum ein Vorteil ist, dieser positive Effekt in normalem Leitungswasser mit moderaten Wasserwerten auf Grund der geringeren Konzentrationsunterschiede zwischen Blutplasma und Wasser aber nicht gebraucht wird.

Ist also der letzte wichtige Parameter, die Keimarmut, der Schlüssel zu den Problemen bei der Eingewöhnung von ausgesprochenen Weichwasserfischen? Die Konzentration oder Dichte an potenziell schädlichen Keimen, in der aquaristischen Literatur auch immer wieder als „Keimzahl“ bezeichnet, wurde in den letzten Jahren wiederholt diskutiert. Wer sich einen Überblick über die Bedeutung dieser Größen für die Aquaristik machen möchte, dem sei die Literatur von einigen Büchern zum Thema Fischkrankheiten (Reichenbach-Klinke 1980, ter Höfte und Arend 1997, Untergasser 1989) und das sehr empfehlenswerte Buch von Bremer über Fischernährung (Bremer 1997) empfohlen. Die relativ hohe Keimbelastung von Aquarienwasser kann dazu führen, dass sich an den Kiemen vieler Fische, dem Ort des Gasaustausches und der Ionenregulation, eine starke Schleimschicht bildet, welche die Funktion der Kiemen stark beeinträchtigen kann. Inwiefern und in welchen Größenordnungen diese Schleimschicht die Prozesse Gasaustausch, pH- und Ionenregulation beeinflusst ist jedoch wissenschaftlich noch nicht vollständig untersucht und schon gar nicht verstanden.
Keimarmut
Wieso ist aber das Schwarzwasser besonders bakterienarm? Auf Grund ihrer Physiologie sind viele Bakterien nur dann in der Lage optimal zu wachsen, wenn der pH im Umgebungsmedium innerhalb gewisser Grenzen optimal eingestellt ist. Der optimale pH für viele Bakterien befindet sich in leicht alkalischen Bereich von pH 7.2 bis 7.8 (Schlegel 1992). Bakterien wachsen auch dann besonders gut, wenn im umgebenden Milieu genügend Ionen und organische Stoffe für den Aufbau von Körpersubstanz vorliegen. Das funktioniert in fast destilliertem saurem Wasser nicht.
Kurzum, ein organisch verschmutztes, leicht alkalisches mittelhartes Leitungswasser mit dauernd zugeführten organischen Nährstoffen und Ionen (aus dem Fischfutter und der Mineralisation von Abfallstoffen), stellt ein optimales Siedlungssubstrat für viele Bakterien dar. Viele Huminsäuren besitzen hingegen für Bakterien wachstumshemmende Eigenschaften. Bakterien wachsen also besonders schlecht in stark mit Huminsäuren angereicherten sehr weichen und sauren Gewässern. Es liegen also im Schwarzwasser gerade die umgekehrten Verhältnisse zum „normalen“ Aquarienwasser vor. Nitrat findet sich z.B. im Schwarzwasser Amazoniens nur in Konzentrationen von ca.35 µg l-1, Phosphat im Bereich von ca. 6 µg l-1, also bis zum Faktor 1000 weniger als in Aquarien (Willmer et al. 2005). Schwarzwasser besitzt demnach alle Voraussetzungen dafür, den darin siedelnden Bakterien ein extrem ungünstiges Milieu zur Verfügung zu stellen. Für Bakterien stellt die Zusammensetzung des Schwarzwassers also einen deutlichen Nachteil dar. Diese Erkenntnis ist aber nicht neu, sondern wurde interessanterweise schon von Rolf Geisler vor über 60 Jahren, damals leider ohne Angabe von Zitaten, zur Diskussion gestellt (Geisler 1954).

Es stellt sich jetzt natürlich die Frage, wieso dann in der Natur einige Fischarten ausgerechnet mit dem Schwarzwasser einen aus der Sicht der Fische recht lebensfeindlichen Biotop besiedelt haben. Mit den Wasserwerten bzw. Wasserparametern, wie sie für uns einfach zu bestimmen sind, besitzen wir die Möglichkeit, einige Größen zu bestimmen. Ob wir aber damit in jedem Fall alle Parameter, die einen Biotop charakterisieren, auch charakterisieren können, wage ich zu bezweifeln. Diese Frage kann hier natürlich nicht abschließend geklärt werden, darüber sollten Ökologen, Populationsbiologen und Physiologen sich gemeinsam Gedanken machen. Einige Ansätze oder Anhaltspunkte zum Nachdenken sind sicher die beschränkte Anzahl an ökologischen Nischen und Mikrohabitaten sowie Verdrängungsmechanismen, welche die Tiere zum Besiedeln von extremen Lebensräumen geradezu nötigen.
Fische besiedeln Schwarzwasser nicht, weil sie es wollen, sondern weil sie es können!
Eine mögliche pragmatische Erklärung wäre dann, dass die Fische aufgrund ihrer Anpassungen in diesen Biotope existieren können. Die Art, die physiologisch besonders gut an die Ionenarmut und den niedrigen pH angepasst ist, ist der Art, die im Schwarzwasser die gleichen ökologischen Nischen besiedeln würde, eine Schritt voraus.

Ein kleiner Hinweis noch zum Thema Anpassung: Immer wieder wird behauptet, Schwarzwasserfische hätten sich im Laufe der Evolution an ihre Biotope angepasst und „bräuchten“ deshalb genau dieses Wasser. Andererseits hört man gerade aus aquaristischen Kreisen auch immer, Nachzuchten (F1, F2 oder erst F1000?) wären deutlich toleranter gegenüber den Wasserwerten als Wildfänge: ein extremer Widerspruch? Die gleiche Frage stellt sich, warum „eingewöhnte“ Wildfänge vom Großhändler „stabiler stehen“ als frisch importierte Tiere. Haben die sich womöglich innerhalb von zwei Wochen schon an die dort herrschenden Wasserwerte angepasst?
Fische aus Amazonien können ihre Kiemen innerhalb weniger Tage auf die Umgebung einstellen. Das scheint ein verbreitetes Phänomen zu sein: Auch Lachse oder Aale brauchen nur wenige Tage, um bestimmte Zellen in ihre Kiemen dem Süßwasser bzw. Meerwasser anzupassen.
Wissenschaftliche Untersuchungen der Regulationsfähigkeit von Fischen beim Umsetzen in extreme Gewässer zeigten in der Tat, dass solche Anpassungsleistungen beim Umsetzen von weichem in hartes Wasser (korrekt: ionenarmem in ionenreicheres Wasser) und umgekehrt sehr schnell, oft innerhalb von Stunden vonstatten gehen und meist nach drei bis vier Tagen abgeschlossen sind (Wood et al. 2002, Wang et al. 2003, Gonzalez und Wilson 2001). Von einer evolutiven Anpassung im Zeitraum von vielen Generationen kann deshalb also im Zusammenhang mit Ionen- und pH-Regulation keine Rede sein.
Von einigen Aquarianern hatte ich auch die praktischen Beobachtungen zugetragen bekommen, dass ein Umgewöhnen von Fischen aus weichem in hartes Wasser sehr viel einfacher sei als umgekehrt. Eine Beobachtung, die physiologisch relativ einfach zu erklären ist: Funktioniert die Ionenregulation sehr gut in weichem ionenarmen Wasser, so funktioniert sie auch in hartem ionenreichem Wasser, da die Ionenpumpen leistungsfähig sind und mit den geringen Anforderungen zurechtkommen. Werden aber Fische, die lange Zeit in ionenreichem Wasser gehalten wurden, schnell in weiches Wasser umgesetzt, so müssen sich die Ionenregulationsprozesse erst auf den neuen Gewässertyp umstellen, was einige Zeit bzw. mehrere Tage dauert.
Korrelation und Kausalität
Es sollte nach den obigen Ausführungen klar sein, dass die extreme Ionenarmut und der sehr niedrige pH Faktoren des Schwarzwassers sind, die für die Ionen- und pH-Regulation der Fische nicht positiv zu bewerten sind. Besonders kleine Schwarzwasserfische „brauchen“ also primär nicht unbedingt weiches und saures Wasser, sind aber auf die sekundären positiven Effekte des Schwarzwassers wie z.B. auf die geringe Keimdichte angewiesen. Diese Keimbelastung stellt aber möglicherweise für die Gesundheit der Schwarzwasserfische eine weitaus größere Bedrohung dar als der niedrige pH und die Ionenarmut. Inwiefern Schwarzwasserfische in extrem keimarmem Leitungswasser genauso gut (oder eventuell sogar noch besser?) existieren können wie im künstlich hergestellten Schwarzwasser bedarf genauer verlässlicher und reproduzierbarer Untersuchungen. Möglicherweise ist die Keimdichte im Aquarienwasser eine der wichtigsten, bisher vernachlässigten Wasserparameter für die Pflege unserer Fische.

Wissenschaftlich betrachtet spricht demnach absolut nichts dagegen, Fische, die ursprünglich aus Weichwassergebieten stammen, auch in deutlich ionenreicherem Wasser zu halten, falls es auch mit anderen Möglichkeiten als durch Reduktion der Ionenkonzentration, niedrigen pH-Werten und Zugabe von Huminsäuren möglich ist, die Belastung durch Keime und Abbauprodukte sehr gering zu halten. Biologische Möglichkeiten sind sehr (!) geringer Besatz und wenig Futter. Technische Möglichkeiten dazu bieten zum Beispiel die Ozonisierung und die UV-Behandlung des Wassers nach der Filterung.

Um nicht missverstanden zu werden: Man kann die „natürlichen“ Wasserbedingungen im Aquarium auch nachahmen und kommt mit „Schwarzwasserbecken“ sicher seltener zu Problemen durch Keimbelastungen. Das sollte aber nicht dazu führen, die Wasserhygiene bzw. den Wasserwechsel zu vernachlässigen – weil die Herstellung von Schwarzwasser deutlich aufwendiger ist, als Leitungswasser zu verwenden. Zur Zucht – aber darüber ging der obige Artikel nicht – kommen offenbar ganz andere Faktoren zum Tragen. Und nicht zuletzt hat ein Schwarzwasseraquarium auch seinen ganz besonderen Reiz …
Literatur
Born, H. (1956). Betrachtungen über das “Schwarzwasser” im Aquarium. Die Aquarien und Terrarien-Zeitschrift (DATZ) 9 (9): 237-238.
Bremer, H. (1997). Aquarienfische gesund ernähren. Ulmer-Verlag, Stuttgart; 191 Seiten.
Dejours, P. (1975). Principles of Comparative Respiratory Physiology. NORTH-HOLLAND PUBLISHING COMPANY, Amsterdam Oxford; 253 Seiten.
Evans, D. H., Piermarini, P. M. und Choe, K. P. (2005). The multifunctional fish gill: Dominant site of gas exchange, osmoregulation, acid-base regulation, and excretion of nitrogenous waste. Physiological Reviews 85 (1): 97-177.
Evans, D. H. (1981). Salt and water exchange across vertebrate gills. In Gills, (Hrsg. D. F. Houlihan, J. C. Rankin et al. ), Seite(n) 149-172. Cambridge University Press, CAMBRIDGE.
Fernandes, M. N. und Perna-Martins, S. A. (2002). Chloride cell responses to long-term exposure to distilled and hard water in the gill of the armored catfish, Hypostomus tietensis (Loricariidae). Acta Zoologica 83 (4): 321-328.
Geisler, R. (1953). Beiträge zur Wirkung des Torffilters. Die Aquarien und Terrarien-Zeitschrift (DATZ) 6 (1): 11-13.
Geisler, R. (1954). Das Wasser in den Tropen und in unseren Aquarien. Die Aquarien und Terrarien-Zeitschrift (DATZ) 7 (6): 150-154.
Geisler, R. (1955). Das Wasser aus der Heimat des Neonfisches in Peru. Die Aquarien und Terrarien-Zeitschrift (DATZ) 8 (1): 17-18.
Geisler, R. (1964). Wasserkunde für die aquaristische Praxis. Kernen-Verlag, Stuttgart; 143 Seiten.
Geisler, R. (1972). Im Land des roten Neon. Aquarien Magazin 6 (2): 64-71.
Gonzalez, R. J., Dalton, V. M. und Patrick, M. L. (1997). Ion regulation in ion-poor acidic water by the blackskirt tetra (Gymnocorymbus ternetzi), a fish native to the Amazon River. Physiological Zoology 70 (4): 428-435.
Gonzalez, R. J. und Preest, M. R. (1999). Ionoregulatory specializations for exceptional tolerance of ion-poor, acidic waters in the neon tetra (Paracheirodon innesi). Physiological and Biochemical Zoology 72 (2): 156-163.
Gonzalez, R. J. und Wilson, R. W. (2001). Patterns of ion regulation in acidophilic fish native to the ion-poor, acidic Rio Negro. Journal of Fish Biology 58 (6): 1680-1690.
Gonzalez, R. J., Wilson, R. W., Wood, C. M., Patrick, M. L. und Val, A. L. (2002). Diverse strategies for ion regulation in fish collected from the ion-poor, acidic Rio Negro. Physiological and Biochemical Zoology 75 (1): 37-47.
Hetz, S. K. (2003). Weichwasserfische und ihre Probleme. Aquaristik Fachmagazin (AF) 35 (171): 109-110.
Hirata, T., Kaneko, T., Ono, T., Nakazato, T., Furukawa, N., Hasegawa, S., Wakabayashi, S., Shigekawa, M., Chang, M. H., Romero, M. F. und Hirose, S. (2003). Mechanism of acid adaptation of a fish living in a pH 3.5 lake. American Journal of Physiology 284 (5): R1199-r1212.
Kuchler, I. L., Miekeley, N. und Forsberg, B. R. (2000). A contribution to the chemical characterization of rivers in the Rio Negro Basin, Brazil. Journal of the Brazilian Chemical Society 11 (3): 286-292.
Kirschner, L. B. (1981). Physical basis of solute and water transfer across gills. In Gills, (Hrsg. D. F. Houlihan, J. C. Rankin et al. ), Seite(n) 63-76. Cambridge University Press, CAMBRIDGE.
Laurent, P. und Dunel, S. (1980). Morphology of gill epithelia in fish. American Journal of Physiology 238 (3): R147-59.
Moron, S. E., Oba, E. T., De Andrade, C. A. und Fernandes, M. N. (2003). Chloride cell responses to ion challenge in two tropical freshwater fish, the erythrinids Hoplias malabaricus and Hoplerythrinus unitaeniatus. Journal of Experimental Zoology A 298 (2): 93-104.
Nikinmaa, M. (2001). Haemoglobin function in vertebrates: evolutionary changes in cellular regulation in hypoxia. Respiration Physiology 128 (3): 317-329.
Pelster, B. und Decker, H. (2004). The Root effect – a physiological perspective. Micron 35 (1-2): 73-74.ref_end
Perry, S. F., Shahsavarani, A., Georgalis, T., Bayaa, M., Furimsky, M. und Thomas, S. L. (2003). Channels, pumps, and exchangers in the gill and kidney of freshwater fishes: Their role in ionic and acid-base regulation. Journal of Experimental Zoology A 300a (1): 53-62.
Perry, S. F. (1997). The chloride cell: structure and function in the gills of freshwater fishes. Annual Review of Physiology 59 325-347.
Reichenbach-Klinke, H.-H. (1980). Krankheiten und Schädigungen der Fische. GUSTAV FISCHER VERLAG, Stuttgart, New York; 472 Seiten.
Schlegel, H. G. (1992). Allgemeine Mikrobiologie. Georg Thieme Verlag, Stuttgart, New York; 634 Seiten.
TerHöfte, B. und Arend, P. (1997). Frickhingers Gesund wie der Fisch im Wasser? Tetra-Verlag, Melle; 192 Seiten.
Untergasser, D. (1989). Krankheiten der Aquarienfische: Diagnose und Behandlung. Kosmos-Verlag, Stuttgart; 176 Seiten.
Wang, Y. X., Gonzalez, R. J., Patrick, M. L., Grosell, M., Zhang, C. G., Feng, Q. A., Du, J. Z., Walsh, P. J. und Wood, C. M. (2003). Unusual physiology of scale-less carp, Gymnocypris przewalskii, in Lake Qinghai: a high altitude alkaline saline lake. Comparative Biochemistry and Physiology A 134 (2): 409-421.
Wilkie, M. P. (2002). Ammonia excretion and urea handling by fish gills: Present understanding and future research challenges. Journal of Experimental Zoology 293 (3): 284-301.
Willmer, P., Stone, G. und Johnston, I. (2005). Environmental Physiology of Animals. BLACKWELL PUBLISHING, Malden; 754 Seiten.
Withers, P. (1992). Comparative Animal Physiology. Saunders College Publishing, Orlando; 949 Seiten.
Wood, C. M., Matsuo, A. Y., Wilson, R. W., Gonzalez, R. J., Patrick, M. L., Playle, R. C. und Val, A. L. (2003). Protection by natural blackwater against disturbances in ion fluxes caused by low pH exposure in freshwater stingrays endemic to the Rio Negro. Physiological and Biochemical Zoology 76 (1): 12-27.
Wood, C. M., Wilson, P., Bergman, H. L., Bergman, A. N., Laurent, P., Otiang’a-Owiti, G. und Walsh, P. J. (2002). Ionoregulatory strategies and the role of urea in the Magadi tilapia (Alcolapia grahami). Canadian Journal of Zoology-revue Canadienne De Zoologie 80 (3): 503-515.
